TRAUMATISMO CRANEOENCEFALICO Y VENTILACIÓN MECÁNICA.

El traumatismo craneoencefálico (TCE) es una importante causa de morbimortalidad en cualquier lugar del mundo; afecta más a varones jóvenes y genera un problema de salud pública. Desafortunadamente, los avances en los conocimientos fisiopatológicos no han ido seguidos de similar desarrollo en las opciones terapéuticas, y no se dispone en la actualidad de fármacos neuroprotectores contrastados.
EPIDEMIOLOGÍA:
- Es la primera causa de muerte e incapacidad en la población menor de 45 años en los países desarrollados.
- El Trauma cráneo encefálico el 10 % serán graves, la mortalidad se aproxima al 50 % y el tratamiento sólo la reduce ligeramente.
- El 70% tienen una buena recuperación, el 9% fallecen antes de llegar al hospital, el 6% lo hacen durante su estancia hospitalaria, el 15% quedan funcionalmente incapacitados en diferentes grados (moderados, graves o vegetativos).
- La incidencia es mayor entre los hombres, con una relación hombre/mujer de 3 a 1. Sobre todo afecta a pacientes entre 15 y 25 años.
- Hay otros dos picos importantes: en la infancia y en las personas mayores de 65 años.
ETIOLOGÍA:
- Accidentes de trafico
- Caídas de diferentes alturas
- Traumatismos con objetos contundentes
- Accidentes laborales
CLASIFICACIÓN UTILIZANDO LA ESCALA DE GLASGOW (GCS)
Trauma cráneoencefálico leve: Pérdida de conocimiento menor de 15 minutos y un GCS después de la reanimación cardiopulmonar inicial de 14-15 puntos. Paciente asintomático o con cefalea leve y exploración neurológica normal, Contusión craneal.
Trauma cráneoencefálico moderado: Pérdida de conocimiento mayor de 15 minutos y un GCS después de la reanimación cardiopulmonar inicial de 9-12. Vómitos persistentes, Cefalea intensa, Intoxicación etílica o por drogas, Imposibilidad de realizar historia clínica, Crisis comicial post-traumatismo sin antecedentes de epilepsia, Vértigo postraumático.
Trauma cráneoencefálico grave: Lesión con pérdida de conciencia por más de 6 horas y un GCS después de la reanimación cardiopulmonar de 8 o menos. Focalidad neurológica, Fractura hundimiento,Signos de fractura de base de cráneo, Lesión penetrante o abierta.
FISIOPATOLOGÍA
El TCE es un proceso dinámico, esto implica que el daño es progresivo y la fisiopatología, cambiante incluso hora a hora. Se produce daño por lesión primaria inmediatamente tras el impacto debido a su efecto biomecánico; en relación con el mecanismo y la energía transferida, se produce lesión celular, desgarro y retracción axonal y alteraciones vasculares. Depende de la magnitud de las fuerzas generadas, su dirección y lugar de impacto. Hay lesiones focales como la contusión cerebral, en relación con fuerzas inerciales directamente dirigidas al cerebro y lesiones difusas, como la lesión axonal difusa, en relación con fuerzas de estiramiento, cizallamiento y rotación.
La lesión cerebral secundaria se debe a una serie de procesos metabólicos, moleculares, inflamatorios e incluso vasculares, iniciados en el momento del traumatismo, que actúan sinérgicamente. Se activan cascadas fisiopatológicas, como el incremento de la liberación de aminoácidos excitotóxicos, fundamentalmente glutamato, que a través de la activación de receptores MNDA/AMPA alteran la permeabilidad de membrana aumentando el agua intracelular, liberando potasio al exterior y produciendo la entrada masiva de calcio en la célula. Este calcio intracelular estimula la producción de proteinasas, lipasas y endonucleasas, lo que desemboca en la muerte celular inmediata, por necrosis con respuesta inflamatoria, o diferida, sin inflamación, por apoptosis celular. Se produce activación del estrés oxidativo, aumento de radicales libres de oxígeno y N2, y se produce daño mitocondrial y del ADN.
Tratamiento inicial del traumatismo Craneoencefálico grave.
INTERVENCIÓN INMEDIATA DEL TRAUMA CRÁNEO ENCEFÁLICO SEVERO EN UNIDAD DE CUIDADOS INTENSIVOS.

OBJETIVO
Proporcionar información pertinente a través de la correlación entre artículos científicos encontrados en diferentes bases de datos, acerca de la intervención inmediata dentro de la unidad de cuidados intensivos al paciente con trauma cráneo encefálico.
INTRODUCCIÓN
El paciente politraumatizado es uno de los problemas más graves a los que se enfrenta la sociedad moderna, al tiempo que constituye la cuarta causa de muerte de manera general, solo superado por las enfermedades cardiovasculares, neoplásicas y cerebrovasculares. Asimismo, es la primera entidad causal de mortalidad, en una población con una edad media inferior a los 45 años. Su principal causa son los accidentes de tránsito, que al asociarse con la ingestión de bebidas alcohólicas y otros factores de riesgo como el exceso de velocidad en la conducción de vehículos motores, la inobservancia de las leyes del tránsito, aumentan el daño, duplicando el riesgo de accidentes.(José,R.,matanzas &otros-2011).
Las fuerzas por contacto directo o estáticas suelen provocar lesiones focales. Entre las lesiones focales más frecuentes se encuentran:
Hematoma Subdural: colección de sangre localizado por debajo de la duramadre que es una de las capas que envuelve al cerebro. En muchos casos el sangrado es de origen venoso y por tanto de crecimiento lento. Estos hematomas deben vigilarse pues suelen provocan síntomas a medida que aumentan de tamaño.
Hematoma Epidural: colección de sangre por encima de la duramadre. En muchos casos el sangrado es de origen arterial y por tanto decrecimiento rápido. El paciente puede presentar un periodo sin síntomas tras el traumatismo y al cabo de horas desarrollar una serie de síntomas de alarma (náuseas+vómitos, cefalea, desorientación) acompañados en algunos casos de síntomas localizadores como la debilidad hemicorporal o una dilatación pupilar. Este tipo de hematoma es una emergencia neuroquirúrgica.
Hemorragia Subaracnoidea: colección de sangre en el espacio subaracnoideo Contusión cerebral: lesiones en zonas concretas del parénquima cerebral por disrupción del tejido, de los vasos sanguíneos, por isquemia o edema.
EDEMA CEREBRAL
Se da por aumento del parénquima cerebral a expensas del agua, localizado a nivel intersticial o intracelular; ambos producen un aumento de la presión intracraneal por desequilibrio continente-contenido. Pueden presentarse principalmente dos tipos de edema:
• Edema vasogénico: Por disrupción de la barrera hematoencefálica. En el acto traumático hay liberación de diferentes sustancias como la histamina, el ácido glutámico, serotonina, que van a alterar los sistemas de transporte endoteliales y permiten la salida hacia el espacio intersticial de líquidos y solutos. El edema vasogénico difunde fácilmente a través de la sustancia blanca, probablemente debido a la particular disposición de sus fibras nerviosas y a la baja densidad de capilares.
• Edema citotóxico: Hay alteración de la permeabilidad de la membrana celular, sobre todo de los astrocitos, que produce un paso de líquidos hacia el interior de las células desde el espacio intersticial. El término «edema citotóxico» describe la alteración de la osmorregulación celular. El mecanismo primario parece ser una alteración de la bomba de ATP Na+/K+ dependiente y en el mecanismo de regulación del Ca2+ intracelular, que llevan a la incapacidad de mantener un metabolismo celular normal.
Métodos diagnósticos:
- Escala de Coma de Glasgow
- TAC: permite la detección rápida de lesiones en la bóveda craneana y el encéfalo y es una herramienta invaluable en la guía del tratamiento. La desviación de la línea media se evalúa en la TAC mediante el trazado de una línea transversal desde el borde interno de un lado al otro del cráneo, que pase a nivel del agujero de Monro y una segunda línea desde el borde interno del cráneo (contralateral a la lesión ocupante de espacio) hasta el septum pelucidum , el cálculo de la desviación resulta de la fórmula: DLM = (A/2)-B.364 Para determinar la magnitud de la compresión de las cisternas mesencefálicas por lesiones con efecto de masa o por edema cerebral, se procede a dividir las cisternas en tres ramas: una posterior y dos laterales.
El nivel de conciencia es un excelente indicador de la gravedad de la lesión. La somnolencia, el estupor y el coma son expresiones que indican niveles decrecientes del nivel de conciencia, e indican lesiones de distinta magnitud en uno o ambos hemisferios cerebrales, o en el sistema activador reticular ascendente. Es fundamental realizar un examen sistemático y detallado de los nervios craneanos porque a través de ellos se evalúan estructuras intracraneanas cuyas alteraciones muchas veces no pueden ser determinadas por medio de las maniobras posturales.
Lesiones cerebrales secundarias de causa sistemática:
Se desarrolla posterior al trauma y de forma indirecta. Pueden ser las previamente referidas en que la causa está en el propio cerebro, pero también puede haber causas sistémicas que ocasionan lesión cerebral secundaria por un traumatismo craneoencefálico:
Hipoxia: por obstrucción de la vía aérea, traumatismo torácico, depresión del centro respiratorio, broncoaspiración, neumonías, etc.; se traduce en una eliminación excesiva o un acúmulo de CO2 . Ambos extremos son negativos para el cerebro.
Hipotensión arterial: especialmente grave cuando llega a fallar la autorregulación del FSC por una caída excesiva de la presión de perfusión cerebral. Puede ocurrir en casos de choque hipovolémico, falla circulatoria, etc.
Hipercapnia: provoca vasodilatación, congestión cerebral y aumento de la presión intracraneal. La hipocapnia provoca vasoconstricción, que ocasiona isquemia cerebral.
Hipertermia: Empeora los efectos de la isquemia cerebral.
Alteraciones de la glucemia: Se consideran negativas tanto la hipoglicemia como la hiperglicemia. Su presencia aumenta el riesgo de morbimortalidad, probablemente por un aumento de la producción de radicales libres, edema cerebral, liberación de aminoácidos excitatorios y acidosis cerebral.
Lesión Pulmonar Aguda: Una de las principales complicaciones asociadas al paciente con TCE grave, tanto por su frecuencia como por su gravedad, es la lesión pulmonar aguda. La lesión pulmonar aguda (LPA) se define como la presencia de hipoxemia con independencia de la PEEP aplicada, infiltrados pulmonares bilaterales en la radiografía de tórax y ausencia de signos de patología cardiovascular (o presión capilar pulmonar inferior a 18 mmHg). La aparición de LPA en un paciente con TCE grave empeora ostensiblemente el pronóstico, ya que se triplica el riesgo de muerte y de permanencia en estado vegetativo.
La hiponatremia: Es una complicación común de la enfermedad intracraneal y está asociada a una variedad de trastornos que incluyen al TCE, los tumores cerebrales y las infecciones. La hiponatremia produce edema cerebral, con el consecuente incremento de presión intracraneal.
Ingreso a UCI
El ingreso en UCI será precoz, controlando posición, temperatura, agitación, dolor y hemodinámica, así como la aparición de daño pulmonar, frecuente en estos pacientes. La sedoanalgesia es obligada, y es necesario el control respiratorio y hemodinámico (Alted, et al; 2009).
Medidas generales:
Unidad de Cuidado Intensivos
En la UCI se debe tener en cuenta el:
Medidas Generales para controlar el aumento de la PIC en el TCE
Destete de la ventilación mecánica invasiva y Extubación
Nuevas perspectivas:
INTRODUCCIÓN:

Objetivos
Se controlará estrictamente: temperatura, glucemia, crisis comiciales y sepsis (control metabólico inicial). Deberá mantenerse:
– Normotermia (sin calentamiento activo, control de la hipertermia con fármacos o mecánica)
– Posición alineada y con elevación de la cabeza para mejorar la función pulmonar.
– Control del dolor y la agitación.
– Control hemodinámico con presión arterial sistólica (PAS) _ 120 mmHg.
– Sedación (un 17-20% si hay actividad convulsiva).
– Disminución del daño tisular (movilidad, control de disfunción orgánica y síndromes compartimentales).
Con frecuencia hay daño pulmonar por alteración de ventilación/perfusión (V/Q) por redistribución de la perfusión regional, microembolias, síndrome de respuesta inflamatoria sistémica (SIRS), pérdida de surfactante por hiperventilación y/o actividad simpática, atelectasias, etc (Alted, et al; 2009).
Dos actitudes son tenidas en cuenta:
- Extubación precoz tras periodo vulnerable (valoración diaria de esta posibilidad);
- Ventilación protectora. Hay evidencia que indica que se debe utilizar la ventilación protectora, con bajos volúmenes tidales. Los pacientes ventilados con volúmenes mayores tienen una mayor frecuencia de lesión pulmonar aguda.
Se pueden asociar otros factores que también elevan la incidencia de lesión pulmonar, algunos intracraneales y otros extracraneales: fármacos vasoactivos, actividad inflamatoria, actividad simpática, etc (Alted, et al; 2009).
VENTILACIÓN MECÁNICA
Los pacientes con TCE grave generalmente son intubados y ventilados mecánicamente. Hipoxia, definida como saturación de O2 <90%, o PaO2 <60 mm Hg, se debe evitar la Hiperventilación profiláctica a una PaCO2 <25 mm Hg, no es recomendada dentro de las primeras 24 horas después de una lesión cerebral traumática severa, ya que puede comprometer aún más críticamente.
Perfusión cerebral reducida. Coles et al. Reportaron que, en pacientes con TCE Severo, la hiperventilación aumenta volumen de tejido severamente hipoperfundido dentro del cerebro lesionado, a pesar de las mejoras en presión de perfusión cerebral (PPC) y la presión intracraneal (PIC). Estas reducciones en la perfusión cerebral regional pueden representar regiones de tejido cerebral potencialmente isquémico.
La hiperventilación excesiva y prolongada da como resultado vasoconstricción cerebral e isquemia. Por lo tanto, la hiperventilación se recomienda solo como una medida temporal para reducir una PIC elevada. Un breve período (15-30 minutos) de hiperventilación, a una PaCO2 30-35 mm Hg es recomendado para tratar el deterioro neurológico agudo que refleja aumento de PIC.
La configuración ventilatoria debe ajustarse para mantener una oximetría de pulso (SpO2) de 95% o más y / o PaO2 de 80 mm Hg o más y lograr normoventilación (eucapnia) con PaCO2 de 35 a 40 mm Hg.
Mascia et al. informó que la ventilación de alto volumen tidal es un predictor independiente y asociado con lesión pulmonar aguda en pacientes con TCE grave. Por lo tanto, ventilación protectora con bajo volumen tidal y la presión positiva espiratoria final moderada (PEEP) ha sido recomendada para prevenir lesión pulmonar asociada al ventilador y aumento de PIC.
Antes de succionar al paciente a través del tubo endotraqueal (TET), se requiere una preoxigenación con una fracción de oxígeno inspirado (FiO2) = 1.0, y se recomienda la administración de sedación adicional para evitar la desaturación y aumento repentino en la PIC.
El efecto de la PEEP en la PIC es significativa solo con nivel de PEEP mayor a 15 cm H2O en pacientes hipovolémicos. Sin embargo debería ser usado, el nivel más bajo de PEEP, generalmente de 5 a 8 cm H2O que mantiene un nivel adecuado de oxigenación y previene el colapso espiratorio final. Una PEEP más alta, hasta 15 cm H2O, puede ser utilizado en casos de hipoxemia refractaria (Haddad & Arabi, 2012).
La mejoría en los resultados comunicados de pacientes con trauma craneoencefalico grave (TCEG) se basa fundamentalmente en cinco pilares:
1. Prevención de la lesión primaria. Neuroprotección.
2. Atención adecuada en el lugar del incidente y durante el transporte (especializado).
3. Protocolos de manejo en UCI entrenada (cuidados neurocríticos).
4. Uso adecuado y precoz de la cirugía, incluida la craniectomía descompresiva.
5. Control o atenuación de los mecanismos de lesión secundaria.
Unidad de Cuidado Intensivos
En la UCI se debe tener en cuenta el:
- Control de la hipoxia cerebral: Todo paciente que tenga una puntuación menor o igual a 8 puntos sera sometidos relajación, intubación y ventilación mecánica como mínimo durante 24 horas.
- Control de la complianza: Existen tres principios: 1. Impedir retenciones del fluido intracraneal, facilitando el retorno venoso, colocando en posición de 20° la cabeza sobre el plano horizontal 2. Evitar que el tubo orotraqueal se enrede alrededor del cuello 3. Limitar la utilización de la PEEP a la indicación de cortocircuito pulmonar dentro del rango 5-10 CmH2o
- Control de la hipertension intracraneal: Una vez disminuida la complianze, la PIC comienza a ascender lo cual constituye un factor para la reducción del flujo sanguíneo cerebral
- Control metabólico: Este se dirige a suprimir la acidosis metabólica.
- Evitar la hipoxia: Establecer un adecuado soporte ventilatorio y monitorización continua de la saturación de O2 y capnografia para: Una Presión de O2 de 100 mmhg y Una presión de CO2 35-40 mmhg
- Mantener la presión perfucion cerebral (PPC): Recién nacido: 40 mmhg, Lactantes: 50 mmhg, Adulto: 60 mmhg
- Normovolemia con ligera hiperosmolaridad sérica: con una adecuada presión venosa central (PVC)adecuada.
- Cabeza en posición neutra y ligeramente elevada (30 %): esta medida está contraindicada en el shock o si se sospecha inestabilidad de la columna cervical, en este caso se puede utilizar la postura antiTrendelemburg.
Recomendaciones:
Los modos de ventilación con garantía de volumen pueden ser una elección racional en estos pacientes para minimizar las variaciones en la PaCO2.
Se debe evitar una alta PaO2, considerando el riesgo de vasoconstricción cerebral hiperóxica y lesión pulmonar hiperóxica. Se puede administrar PEEP de 5-10 cmH2O para prevenir la atelectasia (se ha demostrado que es seguro en estos pacientes).
Se ha recomendado que la traqueotomía temprana debe realizarse para reducir los días de ventilación cuando el beneficio general supera las complicaciones asociadas con el procedimiento (Nivel IIA).
La fracción de ajustes de oxígeno inspirado (FiO2) en un ventilador debe ajustarse para lograr una PaO2 de ~ 90 mmHg, que puede oxigenar la zona de la penumbra.
Destete de la ventilación mecánica invasiva y Extubación
La población de pacientes con lesiones cerebrales severas está en niveles altos riesgo de falla de extubación con tasas de hasta el 38%. Actualmente, no se ha descrito ninguna estrategia con respecto a el destete o la extubación. Las características clínicas y el nivel de activación compatible con éxito de extubación aún se debaten en pacientes con lesión cerebral y, por lo tanto, las tasas de falla de extubación y retraso la de la misma sigue siendo alta en esta población.
El fracaso en la extubación se asocia con una morbilidad significativa: neumonía nosocomial, mayor duración de la ventilación mecánica, mayor duración de la estancia en la UCI y mayor mortalidad, pero la causa de la falla de extubación es probablemente más perjudicial que la falla misma. El miedo al fracaso en la extubación explica la alta tasa de extubación retrasada de los Pacientes en UCI (la extubación se considera como demorada cuando los pacientes no son extubados dentro de las 48 hr de la reunión criterios de preparación definidos), a pesar de retrasar la extubación
El retraso en la extubación conduce a un aumento de la tasa de neumonía alterando el daño neurológico y aumenta los costos de atención médica (Asehnoune et al, 2018).
Cómo configurar la ventilación mecánica en la Práctica clínica. Hubo una reevaluación reciente sobre los efectos de la PEEP en la presión de perfusión cerebral (PPC). En un estudio retrospectivo en 341 pacientes, los autores notaron una disminución con significación estadística en la PPC con aumento en PEEP, pero La PPC permaneció dentro del objetivo terapéutico. Por otra parte, no se proporcionaron datos sobre el estado de la enfermedad pulmonar de los pacientes; esto es importante porque la PEEP puede alterar la PPC en condiciones de hipovolemia. En un estudio prospectivo piloto realizado en 20 pacientes con TCE y síndrome de dificultad respiratoria aguda (SDRA), los autores aumentaron la PEEP hasta 15 cmH2O. No hubo cambios significativos en la PIC o en la PPC y, lo que es más importante, los autores informaron una mejoría significativa en la oxigenación del tejido cerebral con niveles más altos de PEEP.
En conclusión, parece que un aumento en PEEP puede ser aplicado con seguridad en pacientes con SDRA con lesión cerebral, siempre que son normovolémicos e incluso pueden tener efectos benéficos cerebrales. Nuestro grupo confirmó recientemente la seguridad de la PEEP al mostrar que PEEP> 5 cmH2O no alteró la PIC en pacientes con lesión cerebral grave. El uso del volumen corriente bajo dentro de estrategia de ventilación protectora en la población en general de UCI es fuertemente asociado con mejores resultados (Asehnoune et al, 2018).
PRESCRIPCIÓN DEL EJERCICIO
INTRODUCCIÓN:
El ejercicio es beneficioso para muchas personas, incluso para alguien que ha sufrido una lesión cerebral traumática (TBI). Se ha demostrado que el ejercicio ayuda a mejorar y prevenir muchas afecciones, entre ellas: control del peso, niveles de estrés, regulación / estado de ánimo emocional, memoria, atención, fortaleza, resistencia, equilibrio, flexibilidad y regulación de la presión arterial. Se ha demostrado que el ejercicio ayuda a prevenir la diabetes tipo II, el accidente cerebrovascular, la enfermedad cardíaca y algunas formas de cáncer. (American Physical Therapy Association (APTA); sf)
Beneficios: Los beneficios del ejercicio pueden ser especialmente útiles después de un TBI ya que muchas personas que han tenido una lesión reportan dificultades en al menos una o más de las siguientes áreas: control de peso, control del estrés, regulación emocional / estado de ánimo, memoria, atención, fortaleza, resistencia y niveles de energía. Los sobrevivientes de TBI que realizaron ejercicio 3 veces por semana durante intervalos de 30 minutos informaron menos depresión, mejoraron su percepción de las capacidades físicas y aumentaron la integración en la comunidad en comparación con los sobrevivientes de TBI que no hicieron ejercicio con regularidad. Los estudios demuestran que el ejercicio regular puede influir positivamente en la capacidad cognitiva y cardiorrespiratoria en personas que han sufrido un TBI. Las investigaciones actuales sugieren que hacer ejercicio entre 20 y 40 minutos 3 a 4 veces por semana ayudará a lograr beneficios óptimos. (American Physical Therapy Association (APTA); sf)
En relación al ejercicio en pacientes con TEC se ha determinado que el ejercicio en si es beneficioso, siendo capaz de aumentar la atención, memoria de trabajo, velocidad de procesamiento, mediante cambios vasculares que optimizan la saturación de oxígeno, promoviendo así la angiogénesis y mejorando el flujo sanguíneo cerebral. (Soto, Claudio et al; 2014).
La función física se refiere a las habilidades sensoriomotoras. Durante la rehabilitación es requerida la realización de actividades de la vida cotidiana e instrumental, estas actividades son habilidades avanzadas y consideradas vitales para la independencia del individuo dentro de la comunidad.
Se recomienda realizar rehabilitación física mediante estiramientos o ejercicios, promover la independencia funcional y realizar estiramientos de muñeca en población adulta con hemiparesia (Soto, Claudio et al; 2014).
PRESCRIPCIÓN DEL EJERCICIO EN UNIDAD DE CUIDADOS INTENSIVOS.

Objetivos
- Mejorar la función cerebral y el aumento del grado de independencia por medio de un tratamiento fisioterapeutico protocolizado.
- Prevenir las complicaciones de la patologías de estos pacientes y las producidas por el encamamiento prolongado en la unidad de cuidado intensivo.
Si no se les hace el correcto tratamiento preventivo se pueden generar úlceras por presión, rigideces articulares, contracturas musculares, que alargan la estancia hospitalaria, pueden producir complicaciones y dificultan la rehabilitación, aumentando su duración y precisando técnicas o tratamientos más costosos, e incluso intervenciones quirúrgicas.
Es necesario que los fisioterapeutas especializados e integrados en el equipo multidisciplinario, Las sesiones de fisioterapia serán breves dependiendo para la prescripción en cada paciente, ya que se va a modificar dependiendo el trauma ya sea leve, modera o grave; Al momento de la atención de fisioterapia se va a tener la modificación de algunos parámetros registrados en el paciente como: Saturación de O2, presión craneal, frecuencia cardíaca y tensión arterial.
Durante el periodo de la rehabilitación pueden producirse varias complicaciones que conducen a discapacidades físicas, cognitivas y otras neurológicas que causas un importante retraso en su mejoría funcional, cada paciente con un Trauma Craneoencefalico presenta una sintomatología propia debido a las múltiples combinaciones de déficit que suelen aparecer en este tipo de lesiones. Por tanto, pueden resultar afectados los sistemas motor, sensitivo
Las técnicas mas utilizadas en fisioterapia son: Cambios posturales, masaje, movilización de los distintos segmentos corporales, estiramientos y técnicas variadas de fisioterapia respiratoria.
Masaje
Efectos mecánicos y reflejos sobre los receptores del dolor:
Obtenemos un aumento del umbral del dolor y por lo tanto efecto analgésico disminuyendo su percepción actuando sobre los distintos agentes lesivos: Sobre sustancias químicas irritantes y proinflamatorias y sobre el edema al favorecer su eliminación y drenaje con el retorno venoso. - Compresión de fibras nerviosas: debidas a músculos contraídos o espasmódicos, al disminuir la tensión en esos músculos se liberará la presión sobre los nervios. Sobre la transmisión neuronal: el dolor se transmite por fibras finas y por lo tanto lentas. Al estimular las fibras más gruesas y rápidas mediante la sensibilización cutánea, conseguimos bloquear la transmisión nociceptiva a nivel central. Interrumpe el circuito del dolor consistente en la contracción mantenida de la musculatura dolorida produciendo nuevamente dolor profundo al disminuir esa tensión muscular.
Efectos mecánicos y reflejos sobre la circulación de la sangre:
En el lugar de aplicación se consigue hiperemia debido a la vasodilatación producida por la liberación de hormonas tisulares y sustancias histaminoides. A nivel general actúa a modo de bomba aspirante e impelente, y conseguimos eliminar edemas y exudados al movilizar los líquidos intersticiales. Disminuye la viscosidad de la sangre y el hematocrito, con lo que, en general, aumenta la fluidez sanguínea. Esto va a favorecer la irrigación de tejidos isquémicos y por lo tanto su nutrición y regeneración.
Movilización Pasiva
Efectos fisiológicos de realizar las movilizaciones en:
Articulaciones: conseguimos la activación sensitiva de los receptores situados en la cápsula y ligamentos que enviarán impulsos a la médula y de ahí a los músculos motores de la articulación. Se obtiene una acción de deslizamiento de las superficies cartilaginosas de la cápsula y el ligamento, tensión de estas estructuras y excitación de la sinovial, obteniendo un fin preventivo (mantenimiento de la amplitud del recorrido articular, mantenimiento de las superficies articulares, distensión de retracciones periarticulares, secreción del líquido sinovial, mantenimiento del esquema corporal). Función circulatoria: favorece el retorno venoso mediante la movilización de las articulaciones sobre todo, a nivel de la articulación tibiotarsiana). Además se produce un aumento de la frecuencia cardiaca por estímulo del sistema nervioso vegetativo.
Función respiratoria: las movilizaciones pasivas torácicas consiguen mantener la movilidad de las articulaciones implicadas en la respiración mejorando con ello la ventilación y la nutrición de los diferentes tejidos.

Movilización Activa:
La actividad de las movilizaciones activas podrán ser realizadas si el usuario está activo ; no podrán ser realizadas si el paciente se encuentra sedado o en coma.
Las movilizaciones activas que se realizan han de ser de tipo isometrico. Son las contracciones isométricas (aquellas en las que la actividad muscular no supone desplazamiento de segmentos puesto que el momento motor y resistente opuesto son iguales). Con estas contracciones se consigue mantener la capacidad dinámica, el tono y la fuerza muscular.
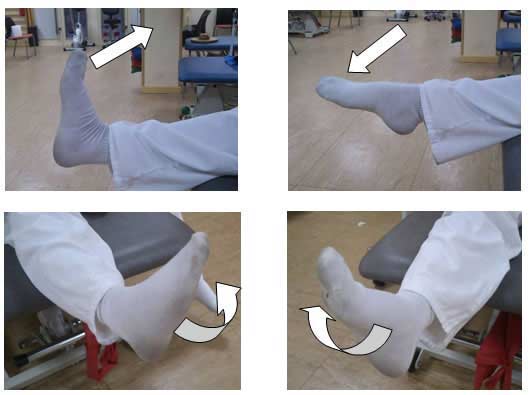
Generalmente se realizan con el músculo en la posición de máximo acortamiento. Siendo útiles:En casos en los que el individuo no puede moverse o trasladarse por si mismo,trabaja el musculo lo más acortado posible para potenciarlo en un determinada acción.
Movilizaciones activas, libres o resistidas:
Se debe trabajar con mayor énfasis en :
Miembros superiores, movilización y fortalecimiento de aquellos grupos musculares implicados ,para el uso inicial de ayudas externas como lo puede ser el uso de muletas, tronco, en la movilización y fortalecimiento de aquellos grupos musculares implicados en la marcha como músculos musculatura del tronco antigravitatoria, así como la encargada del mantenimiento del equilibrio, Miembros inferiores: Movilización y fortalecimiento de musculatura implicada en la marcha. (Sanz.B ;Montona.A;2010).
FASE AGUDA:
Al igual que todo paciente en UCI, el inicio de la terapia física se determinará a partir del diagnóstico fisioterapéutico. No obstante durante la fase inicial en la que el paciente se encuentra sedado, son convenientes las movilizaciones pasivas como estrategia preventiva contra el desacondicionamiento físico . Para esta última existen incluso recomendaciones contra su uso basadas en la evidencia. El ejercicio activo no debería intentarse.
A todo paciente en coma secundario a TCE se le debe iniciar un programa de estimulación multisensorial que incluya estímulos visuales, auditivos, olfatorios y de sensibilidad superficial y profunda . sin embardo Vollman en el 2013 en su artículo “Understanding Critically Ill Patients Hemodynamic Response to Mobilization Using the Evidence to Make It Safe and Feasible” recomienda que se realicen :
- Las aproximaciones articulares: las descargas de peso facilitan los receptores intra articulares permitiendo la aparición de la contracción muscular. Las aproximaciones deben realizarse de distal a proximal.
- Las medidas para prevenir el desarrollo de osificaciones heterotrópicas deben ser implementadas después de la admisión del paciente a la UCI y deben continuar hasta que no haya riesgo alto (recomendación C).
- El mejor tratamiento para las calcificaciones para-articulares es la prevención con un buecontrol postural, con posturas alternas en flexión y extensión periódicas, y movilizaciones articulares frecuentes.
- Para la prevención del hombro doloroso debe considerarse la estabilización en posición neutra de orientación escápulohumeral, usando cabestrillos o cojines axilares y manteniendo el hombro alineado mientras el paciente esté en cama. Los ejercicios para mantener la movilidad articular no deben superar 90 grados de flexión y abducción.
FASE SUB-AGUDA
Ejercicios recomendados: Las intervenciones más frecuentes durante la fase sub-aguda post TCE son:
- La descarga o soporte parcial de peso: La paresia o control motor deficitario se traduce en un deterioro del patrón de marcha. Se postula que el uso de carga parcial sobre las extremidades inferiores permite realizar un entrenamiento precoz, mejorando la fuerza y disminuyendo la espasticidad,
- El manejo específico en transferencias, balance y coordinación han demostrado eficacia y superioridad respecto a los programas tradicionales de entrenamiento muscular.
- Respecto del ejercicio aeróbico, este mejora la capacidad cardiovascular, aumentando la probabilidad de que los pacientes con TEC lo incorporen como hábito, contribuyendo a mejorar la autoestima, el ánimo y la salud mental en general.
PARÁMETRO
|
RECOMENDACIÓN
|
TIPO DE EJERCICIO
|
Baja resistencia, rítmica, dinámica (caminar,
trotar, montar en bicicleta, elíptica)
|
INTENSIDAD
|
60-90% FC Máx
|
DURACIÓN
|
20-40 min por sesión
|
FRECUENCIA
|
3-4 veces por semana
|
Ejercicios específicos:
Es importante adaptar un programa de ejercicios a las necesidades y habilidades específicas de un individuo. Los tipos de ejercicio a considerar incluyen:
- Cardiovascular: este tipo de ejercicio está destinado a aumentar la frecuencia cardíaca, lo que hace que el músculo cardíaco se mantenga fuerte. El ejercicio cardiovascular puede afectar el corazón, los pulmones, la circulación y los músculos. Los ejemplos incluyen: caminar / trotar en una caminadora, pedalear una bicicleta estacionaria, nadar, bailar o hacer clases de aeróbic.
Recomendaciones ejercicio físico aeróbico: Se recomienda actividad física aeróbica, por ejemplo, bicicleta ergométrica, en pacientes con lesión cerebral traumática, durante tres horas y media a la semana, durante el período de doce semanas, mejora el acondicionamiento cardiovascular. Actividad física como caminata o carrera ligera, asociada con fortalecimiento muscular durante tres horas a la semana durante doce semanas también ayuda a mejorar el sistema cardiovascular. El ejercicio aeróbico con fortalecimiento muscular realizado en la piscina terapéutica también resulta en los mismos beneficios.
- Fuerza: este tipo de ejercicio está destinado a desafiar los músculos al empujar o jalar contra la resistencia. El entrenamiento de fuerza también puede influir en la densidad ósea, el equilibrio y la postura de manera positiva. Los ejemplos incluyen: usar pesas libres, usar máquinas de entrenamiento de resistencia, usar tubos / bandas de resistencia.
- Flexibilidad: este tipo de ejercicio está destinado a aumentar la longitud de los músculos y permitir que un individuo mueva sus articulaciones a través de un mayor rango de movimiento. La flexibilidad mejorada puede facilitar el acceso a posiciones como ponerse en cuclillas, doblarse o alcanzar. Los ejemplos incluyen: estiramiento, Tai Chi y yoga.
1. LA PREVENCIÓN Y EL MANEJO DE LAS COMPLICACIONES RESPIRATORIAS: Deben corresponder a un primer objetivo en el proceso de atención del paciente, mediante la terapia respiratoria con técnicas que involucran la movilización de secreciones, el drenaje postural, el reflejo de la tos, la incentivación de la inspiración y espiración, las movilizaciones manuales y cambios de posición.
2. ESTIMULACIÓN MULTISENSORIAL AL PACIENTE EN COMA: Con el fin de estimular al máximo el Sistema Reticular Activante es importante desde el principio mismo de la atención proveer al paciente de estímulos sensoriales de tipo visual, auditivo, olfatorio y de sensibilidad tanto superficial como profunda. Los mismos deben incrementarse en presencia de respuestas y a medida que la recuperación de la conciencia progresa.
3. MANTENER LOS ARCOS DE MOVILIDAD DE TODAS LAS ARTICULACIONES: Mediante movilizaciones pasivas y ejercicios activos cuando es posible. También es importante la reeducación de la función muscular mediante ejercicios de fortalecimiento, ejercicios de estiramiento para prevención de las contracturas y retracciones, y ejercicios de coordinación del movimiento.
Es necesario estirar: Flexores de cadera (sobre todo psoas iliaco en decúbito lateral) y flexores de rodilla con el objetivo de la deambulación correcta. Hombros (mediante de coaptación y circunducciòn de la articulación). Flexores de codo, dedos (proporcionar la funcionalidad de la mano, principal función del miembro superior.
4. TRABAJAR EN EJERCICIOS DE RE-EDUCACIÓN VESTIBULAR Y PROPIOCEPTIVO: Con el fin de lograr un adecuado control del tronco y así permitir inicialmente la sedestación, luego la bipedestación y finalmente la marcha. El entrenamiento de la movilidad debe incluir la movilidad en cama, las transferencias entre la cama y la silla de ruedas, y la marcha independiente o con el uso de ayudas.
Trabajo en Decúbito SUPINO: para la normalización de la musculatura hipertónica del miembro superior, se incluye en esta posición el trabajo del balance articular y muscular de miembros inferiores. Movilización de rótula: ascenso-descenso, lateralizaciones, Cinesiterapia activa y activa-asistida de cadera y rodilla
Movimiento activo-selectivo de la cintura pélvica hacia la extensión de cadera:pedimos a la paciente que eleve la pelvis, manteniendo la posición 10 segundos, incluyendo detenciones del movimiento en el recorrido medio y realizando descansos. De esta forma se produce una activación de los glúteos y de los músculos abdominales
Trabajo en SEDESTACIÓN. con esta posición incluimos una serie de actividades para lograr un mejor control postural del tronco. Paso de decúbito a sedestación: Facilitación del paso de decúbito supino a sedestación contribuyendo a la contracción de la musculatura abdominal. Para incorporarse, el paciente se levantará hacia el lado hemiparésico, apoyando el lado afecto y ayudándose a la incorporación con el lado sano. Trabajo selectivo de Miembros superiores en sedestación: A continuación se proponen diferentes actividades que pueden realizarse tanto en la posición de decúbito
Trabajo de reacciones de enderezamiento, apoyo y equilibrio en sedestación: Control de tronco mientras se realizan rotaciones de cabeza con miembros superiores apoyados en camilla, o bien manos entrelazadas.
Control del tronco con desestabilizaciones empujando desde los hombros para el trabajo de las reacciones de equilibrio.
Rotaciones del tronco en sedestación: Se pueden realizar mediante el uso de objetos tales como aros o pelotas de diferentes tamaños. Pedimos el paso del aro de un lado a otro, además del alcance de objetos a distintas alturas, tanto con el miembro afecto como con ambas manos. A mayor dificultad de alcance que permita la paciente se contribuye a la normalización del tono muscular, además de movimientos basculantes de pelvis, trabajo de extensores de cadera, abductores, y sobre todo trabajo de las reacciones de enderezamiento del tronco.
INTERVENCIÓN FISIOTERAPÉUTICA
Existen complicaciones comunes asociadas particularmente con una estancia prolongada en la UCI, incluyendo desacondicionamiento, hipotensión ortostática, éstasis venoso, reducción de los volúmenes pulmonares, deterioro del intercambio gaseoso, atrofia muscular, contracturas articulares, lesiones de nervios periféricos, zonas de presión y reducción en general del estado de salud, relacionadas con la calidad de vida, las cuales pueden generar una mayor duración de la ventilación mecánica (VM), de la estancia hospitalaria y, por lo tanto, reducir la posibilidad de los pacientes de recuperarse, aumentando así los costos de la intervención. Por esta razón, la inmovilización prolongada se constituye como un factor de riesgo asociado a muchas complicaciones sistémicas.
Se ha llegado a afirmar que después de siete días de soporte ventilatorio, del 25 % al 33 % de los pacientes experimenta debilidad neuromuscular clínicamente evidente, que se considera una causa importante para aumentar el tiempo de su duración y por lo tanto de permanencia en la UCI. Aunque la Fisioterapia es una práctica común en la mayoría de las UCIs, su factibilidad y beneficios, en la aplicación para hacer frente a las secuelas perjudiciales del reposo en cama prolongado, son aún limitados, pues sus intervenciones en esta área suelen ser insuficientes o no se realizan con la rigurosidad necesaria.
Sin embargo, no cabe duda de la mayor atención que se le está dando en ciertos lugares a la actividad física temprana como una modalidad factible después de la estabilización inicial cardio-respiratoria y neurológica del paciente, concluyendo que el posicionamiento, la movilización temprana y el ejercicio, deben ser la primera línea de tratamiento para los pacientes críticos.
La literatura sugiere que la rehabilitación en UCI para pacientes se centra principalmente en las vías respiratorias, terapia de movimiento pasivo-asistencial para evitar contracturas, profilaxis, terapia de estimulación, dosis bajas de fuerza y entrenamiento de resistencia y estiramiento. El objetivo de la terapia física suele estar centrado en la prevención de la daños secundarios (como, neumonía o contracturas), promoción de conciencia y percepción sensorial, y fortalecimiento muscular.(M. Bartolo et al; 2017)
La literatura sugiere que la rehabilitación en UCI para pacientes se centra principalmente en las vías respiratorias, terapia de movimiento pasivo-asistencial para evitar contracturas, profilaxis, terapia de estimulación, dosis bajas de fuerza y entrenamiento de resistencia y estiramiento. El objetivo de la terapia física suele estar centrado en la prevención de la daños secundarios (como, neumonía o contracturas), promoción de conciencia y percepción sensorial, y fortalecimiento muscular.(M. Bartolo et al; 2017)
Efectos de un protocolo de movilización y sedestación progresiva temprana, en la duración de la VM y de estancia en la UCINeurorehabilitación
Según Marqués 2013, las diferentes técnicas que se realizan en fisioterapia respiratoria tienen que ser asignadas por el fisioterapeuta e indicadas de manera individualizada dependiendo de la recuperación del paciente.
 |
| Ramirez,G.(2013)"salida de hospitalización". |
Nivel I: pacientes inconscientes con Glasgow ≤8, con intubación orotraqueal no mayor a 72 horas. Se incluyen movilizaciones pasivas en las articulaciones de las cuatro extremidades y cambios de posición a decúbito lateral. Para los miembros superiores (MMSS) se incluyeron: flexoextensión de dedos, flexo-extensión de muñeca, desviación radial y cubital, flexo-extensión de codo, prono-supinación, flexión, abducción, rotación interna y externa de hombro. Para los miembros inferiores (MMII) se incluyeron: flexoextensión de dedos, dorsiflexión, plantiflexión, inversión y eversión del pie, flexo-extensión de rodilla, flexión, abducción, aducción, rotación interna y externa de cadera.
Nivel II: se incluyeron aquellos pacientes que tuvieran capacidad para interactuar con el terapeuta, determinada por la obtención de mínimo 3/5 respuestas correctas a los siguientes comandos: abra y cierre los ojos, míreme, apriete mi mano, abra la boca y saque la lengua, asienta con la cabeza. Se continuó con las actividades del nivel anterior y se progresó a movilizaciones activo-asistidas y activas, según la capacidad del paciente. Se realizó el paso a sedente largo de forma progresiva (45-90°) en las sesiones, manteniendo la posición mínimo por 20 minutos.
Nivel III: se incluyeron aquellos pacientes que tuvieran una calificación de 3/5 en fuerza de bíceps (ser capaz de mover los MMSS en contra de la gravedad). Se continuó con las actividades del nivel anterior y se progresó a la posición sedente al borde de la cama. En esta posición se trabajaron ejercicios de transferencias de peso y balance.
Nivel IV: se incluyeron aquellos pacientes que tuvieran una calificación de 3/5 en fuerza de cuádriceps (ser capaz de mover los MMII en contra de la gravedad). Se continuó con las actividades del nivel anterior y se realizó la transferencia a una silla, manteniendo la posición mínimo por 20 minutos. Durante la transferencia, se realizaron actividades simples
en posición bípeda (desplazamientos de peso hacia adelante
y hacia los lados) (Segura et al, 2013).
(Denehy, 2008)
El objetivo del tratamiento neurorrehabilitador debe estar orientado a prevenir las complicaciones derivadas de la lesión cerebral, minimizar los déficit físicos, cognitivos y conductuales resultantes, reducir la discapacidad residual, conseguir el mayor grado de integración social, alcanzar la mejor calidad de vida posible dentro de las coordenadas que se establecen por su discapacidad, e informar, formar y entrenar a las familias en los cuidados del paciente.
Etapas de la neurorrehabilitación:
La neurorrehabilitación tiene dos etapas sucesivas, cada una con dos estadios. La primera, intrahospitalaria, es la inmediata a la lesión y precisa atención hospitalaria y servicios de alta especialización y la segunda es extrahospitalaria.Fase intrahospitalaria
Abarca el recorrido inicial intrahospitalario del paciente con lesión cerebral. Tiene dos estadios sucesivos: un período crítico inicial que se sigue de una fase aguda. Fase crítica: es el momento más próximo a la instauración del daño cerebral. Son pacientes todavía portadores de secuelas severas, que están en la fase final de su estancia en UCI o acaban de abandonarla. Están en coma o con secuelas muy severas con afección cognitiva muy importante. Están estables desde el punto de vista hemodinámico y respiratorio y sin complicaciones neuroquirúrgicas urgentes. Tienen un riesgo alto de desarrollar complicaciones derivadas de su lesión cerebral, como crisis comiciales, problemas respiratorios en los portadores de traqueotomías y disfagia. El objetivo inicial es la estabilización clínica y el tratamiento y la prevención de complicaciones.
Programas específicos de rehabilitación inicial intrahospitalaria:
(Odriozola et al, 2009)
De acuerdo con el
estudio realizado por Almeida
TLT, et. al; (2012) Un programa de fisioterapia y terapia
ocupacional, con 6.4 horas / semana de entrenamiento para pacientes con
traumatismo cerebral, es más efectiva en la recuperación de las funciones
motoras, reduciendo en catorce días (p <0,001) el período de permanencia de
los pacientes en la unidad de un centro de rehabilitación.
La intervención
intensiva de un programa de fisioterapia realizado en 9.66 horas / semana (580
minutos), con pacientes después de seis meses a partir de una lesión cerebral
traumática mejora el control del esfínter (p = 0.003), las transferencias (p =
0.05), disminuye los días de internación, promedio de sesenta y dos días (p =
0.03).
de 6.7 horas / semana
(402 minutos). El entrenamiento de rehabilitación con 4 horas / día durante
cinco días a la semana para pacientes con traumatismo moderado a severo en la
fase subaguda, se traduce en una mayor recuperación de la función motora en el
tercer mes de rehabilitación (p = 0.016).
MANEJO VENTILATORIO EN UCI
La ventilación de los pacientes con TCE grave pretende mantener la PCO2
dentro de un rango normal de 34–38 mmHg. Se debe evitar la hipoventilación, ya
que el aumento de los niveles de PCO2 puede provocar hiperemia cerebral con un
aumento del volumen sanguíneo y la PIC. Por otro lado, la hiperventilación
produce un mayor riesgo de vasoconstricción y un aumento de la hipoxia tisular,
especialmente en la zona de penumbra, por lo que es mejor evitarla. La configuración de
la fracción de oxígeno inspirado (FiO2) en un ventilador debe ajustarse para
lograr una PaO2 de ~ 90 mmHg, que puede oxigenar la zona penumbra. Debe
evitarse la alta PaO2 considerando el riesgo de vasoconstricción cerebral
hiperóxica y lesión pulmonar hiperóxica. Se puede administrar PEEP de 5 a 10
cmH2O para prevenir la atelectasia y ha demostrado ser seguro en estos
pacientes. La inhalación de agonistas beta-2 puede inducir vasodilatación
transitoria con aumento de la PIC y reducción en la presión arterial; si esto
ocurre, la dosis debe reducirse a la mitad (Dash and Chavali; 2018).
El manejo respiratorio en general puede tener un impacto neurológico.
Ahora está claro que la PEEP tiene efectos menores en CPP en pacientes
euvolémicos e incluso podría tener consecuencias positivas en la oxigenación
del tejido cerebral, con efecto protector de la ventilación, con bajos
volúmenes corrientes (6–8 ml / kg de peso corporal ideal), se puede realizar
con seguridad después de la lesión cerebral. La extubación sigue siendo un reto
en el ajuste neuro-UCI, esperando la completa neurología del paciente. La
recuperación no es obligatoria y algunas características específicas, tales
como la persecución visual, la tos y la deglución, puede ayudar al médico
tratante a realizar la extubación. La traqueotomía puede ser considerada, pero
el mejor momento y la selección de pacientes que podrían beneficiarse de esto
aún no está clara. (Asehnoune, K; 2018).
EL EFECTO POSITIVO DE LA FISIOTERAPIA RESPIRATORIA EN PACIENTE EN UCI
Según Tenorio, 2012 es importante tener tres objetivos como
fisioterapeuta para disminuir complicaciones en UCI y tener un tratamiento más
efectivo:
1.
Prevención y tratamiento de la atelectasia.
3. Condiciones
relacionadas con el desacondicionamiento físico y deterioro funcional.
La fisioterapia respiratoria favorece la eliminación de las
secreciones mediante aspiración endotraqueal y ayudan a prevenir las
complicaciones relacionadas con la ventilación mecánica, como las infecciones.
También se usan técnicas de reeducación o control de la respiración:
Control respiratorio
Ventilación dirigida
El Protocolo de posicionamiento en cama es importante ya que ayuda
a disminuir las resistencias de la vía aérea, aumenta el trabajo de
los músculos respiratorios (intercostales internos, diafragma).
Control respiratorio
Ventilación dirigida
La diferentes posiciones que se realizan tienen beneficios como:
1. El decúbito prono mejora la oxigenación para algunos
pacientes con fallo respiratorio agudo y distress respiratorio.
2. El decúbito lateral mejora la oxigenación
de algunos pacientes con aumento de la resistencia de la vía aérea.
Es
importante que el estado hemodinámico debe ser siempre monitorizado durante el
tratamiento de fisioterapia para detectar cualquier efecto negativo.
(Ferreira et al, 2013)
TÉCNICAS DE FISIOTERAPIA:
1. Control de la respiración, (respiración diafragmática):
Son periodos de respiración lenta a volumen corriente con relajación de los músculos
accesorios respiratorios y ventilación con el diafragma, intercalados entre técnicas
más activas con el fin de permitir la recuperación y evitar el agotamiento.
2. Percusión torácica: Golpeteo
repetido con la punta de los dedos en lactantes, la mano hueca en niños y
adultos sobre las distintas zonas del tórax. Se combina con el drenaje
postural.
3.Vibración torácica: Se aplican las
manos, o las puntas de los dedos, sobre la pared torácica y sin despegarlas se
genera una vibración durante la espiración. Se combina con la compresión y el
drenaje postural.
4.Tos provocada y dirigida: El
despegamiento de la mucosidad de la pared desencadena habitualmente la tos. En
su defecto, puede provocarse la tos aplicando una suave presión sobre la tráquea
en el hueco supraesternal al final de la inspiración. La tos produce la expectoración
de la mucosidad por la boca o su deglución.
Fase extrahospitalaria.
Más orientada a la reinserción domiciliaria y comunitaria. Depende de forma muy importante de una serie de factores contextuales, entre los que destaca el soporte familiar eficaz. Su ausencia suele implicar un aumento del período de institucionalización. A partir de ese momento los objetivos de la neurorrehabilitación giran, de forma predominante, en torno al concepto de calidad de vida y no en torno a la curación o la supervivencia. Fase subaguda: debe estar vinculada estructuralmente a un servicio de rehabilitación, pero en régimen de hospital de día, porque todavía se puede esperar ganancias funcionales. Favorece el paso de los cuidados hospitalarios a los domiciliarios, vincula al paciente con un centro que facilitará las interconsultas, reduce el tiempo de estancia en las unidades de hospitalización convencionales. Puede durar hasta 1 año. Fase crónica: el paciente está estable neurológica y funcionalmente, pero aún puede beneficiarse de algún programa para aquellos aspectos en que la deficiencia es más discapacitante (logopedia, fisioterapia, neuropsicología). En ocasiones, debe hacerse para no recaer en el deterioro. Dura unos 2 años más (Odriozola et al, 2009).
Emilie I et. al; 2017 refiere que se deben tener en cuenta al momento de la fase extra hospitalaria 3 aspectos importantes para una adecuada intervención :
• Ventilación mecánica. Después de la extubación, oxigenoterapia de acuerdo con resultados de gases arteriales. Uso de técnicas de reexpansión pulmonar instrumentales y no instrumentales de acuerdo con respuesta.
• Mejoramiento de la capacidad aeróbica.
• Mantenimiento de los arcos de movilidad articular y ejercicios terapéuticos para mantenimiento de fuerza muscular.
BÚSQUEDA BIBLIOGRÁFICA
1. Gonzàlez,L& Garcia,A.(2013).
Traumatismo Craneoencefàlico. Revista Mexicana de Anestesiologìa. Vol: 36 N: 1.
PP: 186-193. Instituto Nacional de Neurologìa y Neurocirugia.
2. Pèrez,A., Àlvarez,M., Porto,R &
Caballero,J. (2011). Revisión sobre el manejo del trauma cráneo encefálico en
la Unidad de Cuidados Intensivos Emergentes. Matanzas. Revista mèdica
electrònica. Vol:33(2). PP:225-234.
3. Orbe,B., Arias,R., Martin,R.,
Garcia,C., Moreiro,M., Foncea,A & Gòmez,C. (2006). Revisiòn del traumatismo
craneoencefalico. Vol:17. PP: 495-518.
4. López, E. A., Aznárez, S. B., &
Fernández, M. C. (2009). Actualizaciones en el manejo del traumatismo
craneoencefálico grave. Medicina
intensiva, 33(1), 16-30.
5. Rodríguez-Boto, G., Rivero-Garvía,
M., Gutiérrez-González, R., & Márquez-Rivas, J. (2015). Conceptos básicos
sobre la fisiopatología cerebral y la monitorización de la presión
intracraneal. Neurología, 30(1), 16-22.
6. Alted López E Et Al. (2009). Actualizaciones en el
manejo del traumatismo craneoencefálico grave. Med Intensiva;33(1):16-30.
7. Haddad & Arabi. (2012).
Critical care management of severe traumatic brain injury in adults. Scandinavian Journal
of Trauma, Resuscitation and Emergency Medicine;20:12.
8. Asehnoune et al. (2018).
Respiratory Management in Patients with. Severe
Brain Injury. Critical Care; 22:76
9. Dash & Chavali. (2018). Management of
traumatic brain injury patients. Korean
Journal of Anesthesiology; 71(1).
10.
Soto, Claudio et al. (2014). Aspectos
fundamentales en la rehabilitación post TEC en el paciente adulto y
pediátrico. Rev. Med. Clin. Condes; 25(2): 306-313.
11. Almeida TLT, et
al; (2011). Traumatic brain injury: rehabilitation. Acta Fisiatr; 19(2):130-7.
12. American Physical Therapy Association (APTA). (s.f).
Exercise After Traumatic Brain Injury.
13. Irdesel,J., Aydiner,B & Akgoz,S. (2007). Rehabilitation outcome after traumatic brain injury. Revista neurocirugia. Vol:18 PP: 5-15.
14. Segira, D. C., Martínez, V. L., Herrera, Y. R., Medina, C. R., & Mogollón, P. (2013). Movilización temprana, duración de la ventilación mecánica y estancia en cuidados intensivos. Revista de la Facultad de Medicina, 61(4), 373-379.
15. Odriozola, F. A., Ibarrarán, M. I., Gorostidi, Á. M., Murgialdai, A., & Garde, P. M. (2009). Pronóstico de las secuelas tras la lesión cerebral. Medicina intensiva, 33(4), 171-181.
16. Azeredo CAC. Fisioterapia respiratória. Rio de Janeiro: Panamed; 1984.
17. Malkoç
M, Karadibak D, Yildirim Y. The effect of physiotherapy on ventilatory
dependency and the length of stay in an intensive care unit. Int J Rehabil Res.2009;32(1):85-8.
18. Schimpf MM. Diagnosing increased intracranial pressure. J Trauma Nurs. 2012;19(3):160-7.
19. Zanier ER, Ortolano F, Ghisoni L, Colombo A,
Losappio S, Stocchetti N.Intracranial pressure monitoring in intensive care:
clinical advantages of a computerized system over manual recording. Crit Care.
2007;11(1):R7.
20. Howe, E. I., Langlo, K. P. S., Terjesen, H. C. A., Røe, C., Schanke, A. K., Søberg, H. L., ... & Klethagen, P. (2017). Combined cognitive and vocational interventions after mild to moderate traumatic brain injury: study protocol for a randomized controlled trial. Trials, 18(1), 483.
21. Vollman, K. M. (2013). Understanding critically ill patients hemodynamic response to mobilization: using the evidence to make it safe and feasible. Critical care nursing quarterly, 36(1), 17-27.
22. M. Bartolo et al. (2017). Mobilization in early rehabilitation in intensive care unit patients with severe acquired brain injury: an observational study. J Rehabil Med;49: 715–722.
20. Howe, E. I., Langlo, K. P. S., Terjesen, H. C. A., Røe, C., Schanke, A. K., Søberg, H. L., ... & Klethagen, P. (2017). Combined cognitive and vocational interventions after mild to moderate traumatic brain injury: study protocol for a randomized controlled trial. Trials, 18(1), 483.
21. Vollman, K. M. (2013). Understanding critically ill patients hemodynamic response to mobilization: using the evidence to make it safe and feasible. Critical care nursing quarterly, 36(1), 17-27.
22. M. Bartolo et al. (2017). Mobilization in early rehabilitation in intensive care unit patients with severe acquired brain injury: an observational study. J Rehabil Med;49: 715–722.
23.Almeida TLT, et. al.
(2012). Traumatic brain injury: rehabilitation. Acta Fisiatr;19(2):130-7











